Berita Riau
POLEMIK Obat Mengandung Ranitidine di Riau, Diskes Pastikan sudah Tidak Ada di Puskesmas dan RSUD
Polemik obat mengandung ranitidine di Riau, Dinas Kesehatan atau Diskes pastikan sudah tidak ada di Puskesmas dan RSUD
Penulis: johanes | Editor: Nolpitos Hendri
Dengan demikian, hasil studi tersebut menjadi acuan bagi BPOM untuk memerintahkan industri farmasi pemegang izin edar produk untuk melakukan penarikan kembali (recall) seluruh bets produk dari peredaran.
Selain itu, industri farmasi juga diwajibkan untuk melakukan pengujian secara mandiri terhadap cemaran NDMA, serta menarik produk dengan sukarela apabila kandungan cemaran melebihi ambang batas yang diperbolehkan.
Kepada Kompas.com, Kepala NPOM, Penny K Lukita, mengatakan, pihak industri farmasi atau produsen obat harus melaporkan hasil penarikan ke BPOM.
Adapun tenggat waktu penarikan adalah selama 80 hari kerja.
Untuk menjaga kehati-hatian, Badan POM telah menerbitkan Informasi awal untuk Tenaga Profesional Kesehatan pada 17 September 2019 terkait keamanan produk ranitidin yang terkontaminasi NDMA.
Di Indonesia, ranitidine telah mendapatkan persetujuan sejak tahun 1989.
Biasanya, ranitidine tersedia dalam bentuk tablet, sirup, maupun injeksi.
Berikut daftar obat ranitidine yang ditarik dari peredaran:
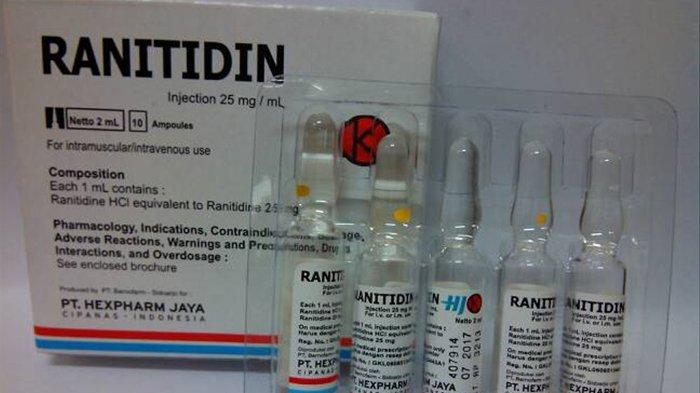
Ranitidine Cairan Injeksi 25 mg/mL, pemegang izin edar PT Phapros Tbk
Nomor Bets Produk Beredar:
95486 160 s/d 190
06486 001 s/d 008
16486 001 s/d 051
26486 001 s/d 018
Zantac Cairan Injeksi 25 mg/mL, pemegang izin edar PT Glaxo Wellcome Indonesia








![[FULL] Ironi Tunjangan Fantastis DPR RI, Pakar: Anggota Dewan Kita Ini Nggak Miskin, Kaya Semua](https://img.youtube.com/vi/bbnwBY3H3qw/mqdefault.jpg)




